Anvisa aprova uso da emergencial da CoronaVac para crianças de 3 a 5 anos
14/07/2022
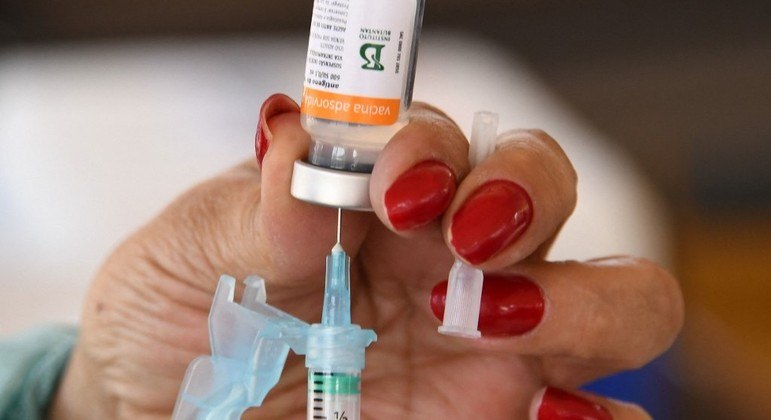
Em reunião extraordinária, a diretoria colegiada da Anvisa (Agência Nacional de Vigilância Sanitária) autorizou nesta quarta-feira (13) o uso emergencial da vacina CoronaVac contra a Covid-19 para crianças de 3 a 5 anos.
A agência levou em consideração que os imunizantes de vírus desativado são usados continuamente no Brasil, como são os casos das vacina contra a gripe e a poliomielite.
“A tecnologia de vírus inativado tem um longo histórico de segurança em vacinas comumente aplicadas em bebês e crianças, assim, apesar das incerteza quanto a eficácia da CoronaVac para evitar que as crianças contraiam a doença, é possível que a CoronaVac seja considerada como estratégia para reduzir os danos da Covid-19”, afirmou Meiruze Sousa Freitas, diretora-relatora da Anvisa.
O esquema vacinal indicado pela área técnica da agência é de duas doses, assim como as aplicadas nos adultos, com intervalo de 28 dias. A vacina não foi recomendada para crianças imunocomprometidas, que são aquelas com deficiência no sistema imune. O fármaco é o mesmo usado em adultos e os frascos seguem iguais.
Na reunião foi salientado que o aumento de número de casos e de mortes por Covid-19 no Brasil e o surgimento de novas variantes capazes de ultrapassar a imunidade colocada pela doença foram essenciais para optar pela aprovação do produto fabricado no Butantan.
Os diretores fizeram a ressalva que a vacina deve seguir sendo objeto de estudo e monitoramento de vida real para verificar a eficácia e a efetividade da resposta imune da CoronaVac à variante Ômicron e possíveis novas variantes do SARS-CoV-2.
Além de que a imunidade celular – resposta imunológica que não envolve anticorpos – produzida pelo imunizante precisa continuar como alvo dos estudos e avaliação do Instituto Butantan.
Até então, o imunizante produzido no Instituto Butantan estava liberado no Brasil para crianças, adolescentes e adultos a partir de 6 anos. Em janeiro desse ano, a agência chegou a negar o pedido de uso para a faixa etária de 3 a 5 anos por falta de dados.
Para aprovação, os especialistas da agência reguladora receberam dados de três estudos feitos no Brasil: Curumim, feito no Espírito Santos; Immunita, do Instituto Butantan com a Fiocruz (Fundação Oswaldo Crus); e Vigvac, também da Fiocruz.
Além disso, foi usado estudo de efetividade da CoronaVac desenvolvido no Chile feito com 500 mil crianças, já convivendo com a alta circulação da variante Ômicron. Nele foi demonstrado uma proteção de 55,06% de efetividade na prevenção de hospitalização de crianças. Foram observadas apenas duas mortes, no grupo de crianças não-vacinadas.
Essa publicação é um oferecimento







